76. NEUROSCIENCE & PSYCHOLOGIE.
La flore intestinale joue un rôle dans la fonction cérébrale et la régulation de l'humeur
Résumé : Un déséquilibre des bactéries intestinales peut entraîner une diminution de certains métabolites, ce qui peut entraîner des symptômes de dépression. Ces résultats fournissent de plus en plus de preuves du rôle du microbiome dans la fonction cérébrale et la santé mentale.
Source: Institut Pasteur
La dépression est un trouble mental qui touche plus de 264 millions de personnes de tous âges dans le monde. La compréhension de ses mécanismes est vitale pour le développement de stratégies thérapeutiques efficaces. Des scientifiques de l'Institut Pasteur, de l'Inserm et du CNRS ont récemment mené une étude montrant qu'un déséquilibre de la communauté bactérienne intestinale peut entraîner une diminution de certains métabolites, entraînant des comportements dépressifs.
Ces résultats, qui montrent qu'un microbiote intestinal sain contribue au fonctionnement normal du cerveau, ont été publiés dans Nature Communications le 11 décembre 2020.
La population bactérienne de l'intestin, connue sous le nom de microbiote intestinal, est le plus grand réservoir de bactéries du corps. La recherche a de plus en plus montré que l'hôte et le microbiote intestinal sont un excellent exemple de systèmes avec des interactions mutuellement bénéfiques. Des observations récentes ont également révélé un lien entre les troubles de l'humeur et les dommages au microbiote intestinal.
Cela a été démontré par un consortium de scientifiques de l'Institut Pasteur, du CNRS et de l'Inserm, qui ont identifié une corrélation entre le microbiote intestinal et l'efficacité de la fluoxétine, molécule fréquemment utilisée comme antidépresseur. Mais certains des mécanismes régissant la dépression, principale cause d'incapacité dans le monde, restaient inconnus.
À l'aide de modèles animaux, des scientifiques ont récemment découvert qu'une modification du microbiote intestinal induite par un stress chronique peut conduire à des comportements de type dépressif, notamment en provoquant une réduction des métabolites lipidiques (petites molécules résultant du métabolisme) dans le sang et le cerveau.
Ces métabolites lipidiques, connus sous le nom de cannabinoïdes endogènes (ou endocannabinoïdes), coordonnent un système de communication dans le corps qui est considérablement entravé par la réduction des métabolites. Le microbiote intestinal joue un rôle dans la fonction cérébrale et la régulation de l'humeur
Les endocannabinoïdes se lient aux récepteurs qui sont également la cible principale du THC, le composant actif le plus connu du cannabis. Les scientifiques ont découvert que l'absence d'endocannabinoïdes dans l'hippocampe, une région clé du cerveau impliquée dans la formation des souvenirs et des émotions, entraînait des comportements dépressifs.
Les scientifiques ont obtenu ces résultats en étudiant les microbiotes d'animaux sains et d'animaux souffrant de troubles de l'humeur. Comme l'explique Pierre-Marie Lledo, Chef de l'Unité Perception et Mémoire à l'Institut Pasteur (CNRS / Institut Pasteur) et co-dernier auteur de l'étude: «Étonnamment, il suffit de transférer le microbiote d'un animal souffrant de troubles de l'humeur à un animal en une bonne santé a suffi à provoquer des changements biochimiques et à conférer à ces derniers des comportements dépressifs.
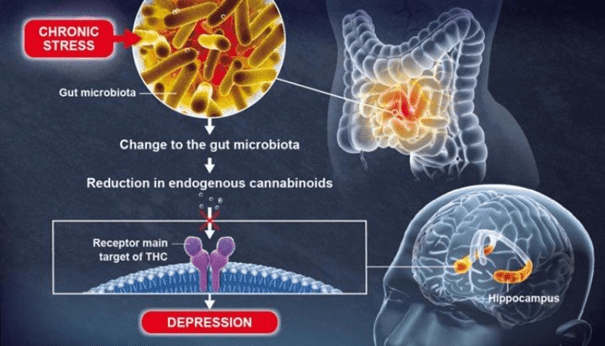
Le microbiote intestinal joue un rôle dans la fonction cérébrale et la régulation de l'humeur. Crédit: Institut Pasteur / Pascal Marseaud
Les scientifiques ont identifié certaines espèces bactériennes qui sont considérablement réduites chez les animaux souffrant de troubles de l'humeur. Ils ont ensuite démontré qu'un traitement oral avec les mêmes bactéries rétablissait des niveaux normaux de dérivés lipidiques, atténuant ainsi les comportements dépressifs. Ces bactéries pourraient donc servir d'antidépresseur. Ces traitements sont appelés «psychobiotiques».
« Cette découverte montre le rôle joué par le microbiote intestinal dans le fonctionnement normal du cerveau», poursuit Gérard Eberl, chef de l'unité Microenvironnement et Immunité (Institut Pasteur / Inserm) et co-auteur de l'étude. S'il y a un déséquilibre dans la communauté bactérienne intestinale, certains lipides vitaux pour le fonctionnement cérébral disparaissent, favorisant l'émergence de comportements dépressifs. Dans ce cas particulier, l'utilisation de bactéries spécifiques pourrait être une méthode prometteuse pour restaurer un microbiote sain et traiter plus efficacement les troubles de l'humeur.
Source: Institut Pasteur
Contact: Aurelie Perthuison - Institut Pasteur
Image: L'image est créditée à l'Institut Pasteur / Pascal Marseaud
Recherche originale: libre accès.
« L'effet du microbiote intestinal sur les comportements dépressifs chez la souris est médiatisé par le système endocannabinoïde » par Grégoire Chevalier, Eleni Siopi, Laure Guenin-Macé, Maud Pascal, Thomas Laval, Aline Rifflet, Ivo Gomperts Boneca, Caroline Demangel, Benoit Colsch, Alain Pruvost, Emeline Chu-Van, Aurélie Messager, François Leulier, Gabriel Lepousez, Gérard Eberl et Pierre-Marie Lledo. Communications de la nature
Abstrait
L'effet du microbiote intestinal sur les comportements dépressifs chez la souris est médié par le système endocannabinoïde
La dépression est la principale cause d'invalidité dans le monde. Des observations récentes ont révélé une association entre les troubles de l'humeur et les altérations du microbiote intestinal. Ici, en utilisant le stress léger chronique imprévisible (UCMS) comme modèle murin de dépression, nous montrons que les souris UCMS présentent des altérations phénotypiques, qui pourraient être transférées des donneurs UCMS aux souris receveuses naïves par transplantation de microbiote fécal. Les altérations cellulaires et comportementales observées chez les souris receveuses étaient accompagnées d'une diminution de la signalisation endocannabinoïde (eCB) en raison de niveaux périphériques inférieurs de précurseurs d'acides gras des ligands eCB. Les effets indésirables du microbiote transféré par l'UCMS ont été atténués en améliorant sélectivement l'eCB central ou par complémentation avec une souche de Lactobacilles genre. Nos résultats fournissent un scénario mécaniste sur la façon dont le stress chronique, le régime alimentaire et le microbiote intestinal génèrent une boucle de réaction pathologique qui contribue au comportement de désespoir via le système central eCB.
Janvier 2021




